
中学教师资格考试(高级化学学科知识与教学能力)模拟试卷67
单项选择题
1.某教师在进行“常见的酸”这一知识点的教学时,首先让学生了解盐酸、硫酸、硝酸、醋酸的性质,然后总结出了酸的通性。该教师运用的主要教学方法是( )。(A)
A. 归纳法
B. 演绎法
C. 实验法
D. 探究法
解析:归纳法是指从实验和观测的事实材料、实验数据出发,推导出一般性结论的方法。演绎法是指从一般规律出发,运用数学的演算或者逻辑的证明,得出特殊事实应遵循的规律即“从一般到特殊”的逻辑推理方法。探究法是学生在教师的指导下,在探究教学实践经验的基础之上,通过创设情境,积极主动地在自主、合作、探究的学习过程中努力地发现问题、提出问题,探寻解决问题的方法和途径,获得终身学习所必备的基础知识和基本技能,学会学习,并形成正确的价值观,从而完成一个教学过程的教学方法。实验法是研究者按照研究目的,以一定的理论假设做指导,合理地控制或创设一定的条件,人为地影响研究对象,从而验证假设,探讨教育现象之间因果关系的一种研究方法。题干中教师运用的主要教学方法是归纳法。
2.要求设计实验证明某种盐的水解是吸热的,有四位同学分别做出如下回答,其中正确的是( )。(D)
A. 甲学生:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
B. 乙学生:在盐酸中加入相同温度的氨水,若实验过程中混合液的温度下降,说明盐类水解是吸热的
C. 丙学生:在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的
D. 丁学生:在醋酸钠溶液中加入酚酞溶液,加热后若红色加深,说明盐类水解是吸热的
解析:因硝酸铵晶体溶于水吸收热量,则水温下降,不能说明盐水解为吸热反应;中和反应为放热反应,且一水合氨的电离过程为吸热反应,不能说明盐类水解是吸热的;醋酸钠溶液中加入醋酸钠晶体,醋酸根离子浓度增大,促进水解,溶解过程伴随热效应,则不能说明盐类水解是吸热的;醋酸钠溶液中滴入酚酞溶液,加热后若红色加深,则说明升高温度可以促进盐类水解,因此可以证明盐类水解为吸热反应。
3.布卢姆认知领域的六种目标中要求层次最高的是( )。(D)
A. 理解
B. 掌握
C. 应用
D. 评价
解析:布卢姆的认知领域分为知识、理解、应用、分析、综合、评价六类目标。其中,评价是认知目标中要求层次最高的。
4.某铁的氧化物(FexO)1.52 g溶于足量稀盐酸中,向所得溶液中通入112 mL标准状况下的Cl2,恰好将Fe2+完全氧化,则x值为( )。(A)
A. 0.80
B. 0.85
C. 0.90
D. 0.93
解析:根据电子守恒可知,FexO被氧化为Fe3+转移的电子数和Cl2转移的电子数相等。标准状况下112 mL Cl2完全反应转移电子数为0.01 mol。则有
5.图1是关于管套实验装置(部分装置未画出)进行的实验,叙述错误的是( )。
 (C)
(C)
A. 利用甲装置可以制取少量H2
B. 利用乙装置(p处放带火星木条,q处伸入水中)可以验证Na2O2与水反应既生成氧气,又放出热量
C. 利用丙装置验证KHCO3和K2CO3的热稳定性,X中应放的物质是K2CO3
D. 利用丁装置制取SO2,并检验其还原性,小试管中的试剂可为酸性KMnO4溶液
解析:利用甲装置,选择试剂锌粒和稀盐酸,可以制取少量H2,A项正确。利用乙装置,p处带火星的木条复燃,说明Na2O2与水反应有氧气产生,q处伸入水中,当反应放出热量时,会导致带支管的锥形瓶中空气受热膨胀,水中有气泡产生,B项正确。KHCO3和K2CO3的热稳定性:K2CO3>KHCO3,玻璃的导热性相对较差,所以应该在外管中放K2CO3,C项错误。利用丁装置,Cu和浓硫酸反应产生SO2,在内管管壁有一小孔,SO2可扩散至内管使酸性高锰酸钾溶液褪色,证明SO2具有还原性,D项正确。
6.某高中化学老师张老师在讲授“氯气”一课时,设计了“七嘴八舌话氯气”的活动,学生兴趣盎然地叙述了许多关于自己对氯气的认识,还提出种种疑问。张老师参与寻找答案的活动,与学生一起通过讨论和实验确定问题的解答。在教学中,他引导学生建立的学习方式是( )。(C)
A. 合作学习、接受学习和体验学习
B. 探究学习、实践研究和巩固学习
C. 自主学习、探究学习和合作学习
D. 自主学习、小组学习和班级学习
解析:
7.在初中化学中,学习化学符号、化学式的相关知识时,适合采用的学习策略是( )。(D)
A. 联系-预测策略
B. 练习反馈策略
C. 可视化策略
D. 多重联系策略
解析:化学符号、化学式的相关知识属于化学用语,学习化学用语时适合采用的学习策略是多重联系策略。
8.化学上常用AG表示溶液中的酸碱度:AG=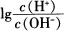 。25℃时,用0.100 mol.L-1的NaOH溶液滴定20.00 mL 0.100
。25℃时,用0.100 mol.L-1的NaOH溶液滴定20.00 mL 0.100
本文档预览:3000字符,共13089字符,源文件无水印,下载后包含无答案版和有答案版,查看完整word版点下载