
中学教师资格认定考试(初级化学学科知识与教学能力)模拟试卷9
单项选择题
1.在中学阶段,下列反应能一步实现的是(C)
A. Al2O3→Al(OH)3
B. NaNO3→NaCl
C. MgO→MgCl2
D. CaCO3→Na2CO3
解析:常见的将Al2O3转化为Al(OH)3的方法是先让Al2O3和酸反应转化为AlCl3,然后再让AlCl2与弱碱反应以制得Al(OH)2,由Al2O3转化为Al(OH)3的化学方程式为Al2O3+6HCl====2AlCl3+3H2O,AlCl3+3NH3·H2O====Al(OH)3↓+3NH4Cl,所以不可一步实现,A项错误。由NaNO3转化为NaCl通常采用的方法是将NaNO3与KCl混合配成溶液,然后采用冷却热饱和溶液法析出KNO3,则剩下溶液里的主要成分就是NaCl,所以不可一步实现,B项错误。由MgO转化为MgCl2可以采用将MgO粉末放入HCl溶液中的方法,可以一步实现,反应的化学方程式为MgO+2HCl====MgCl2+H2O,C项正确。由CaCO3转化为Na2CO3在中学阶段可以采用先让CaCO3与HCl反应生成CO2,然后再将CO2通入NaOH溶液中以制得Na2CO3的方法,反应的化学方程式为CaCO3+2HCl====CaCl2+CO2↑+H2O,CO2(少量)+2NaOH====Na2CO3+H2O,所以不可一步实现,D项错误。
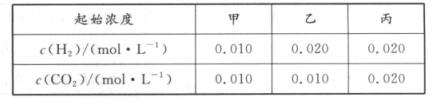
2.某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=9/4。在该温度下向甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),起始浓度如表所示。下列判断不正确的是 ( )
H2O(g)+CO(g)的平衡常数K=9/4。在该温度下向甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),起始浓度如表所示。下列判断不正确的是 ( )
 (C)
(C)
A. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B. 平衡时,甲中和丙中H2的转化率均是60 %
C. 平衡时,乙中CO2的转化率小于60%
D. 平衡时,丙中c(CO2)是甲中的2倍
解析:对于甲容器,设反应的H2的浓度为x mol·L-1可以列三段式进行相关计算:
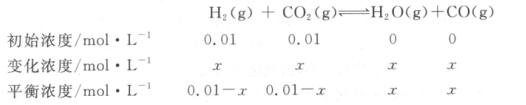 平衡常数
平衡常数 ,解得x=0.006。浓度越大反应速率越快,由表中数据可以知道,甲、乙容器内,开始CO2浓度相等,乙中H2浓度比甲中浓度大,所以速率:乙>甲;乙、丙容器内,开始H2浓度相等,丙中CO2浓度比乙中浓度大,所以速率:丙>乙,故速率:丙>乙>甲,A项正确。甲中H2的转化率为
,解得x=0.006。浓度越大反应速率越快,由表中数据可以知道,甲、乙容器内,开始CO2浓度相等,乙中H2浓度比甲中浓度大,所以速率:乙>甲;乙、丙容器内,开始H2浓度相等,丙中CO2浓度比乙中浓度大,所以速率:丙>乙,故速率:丙>乙>甲,A项正确。甲中H2的转化率为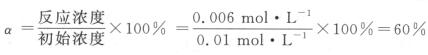 ,甲、丙两容器内起始浓度初始浓度c(H2):c(CO2)=1:1,反应前后体积不变,恒温、恒容下,甲、丙为等效平衡,则丙容器中H2的转化率为60%,B项正确。甲中CO2的转化率为
,甲、丙两容器内起始浓度初始浓度c(H2):c(CO2)=1:1,反应前后体积不变,恒温、恒容下,甲、丙为等效平衡,则丙容器中H2的转化率为60%,B项正确。甲中CO2的转化率为
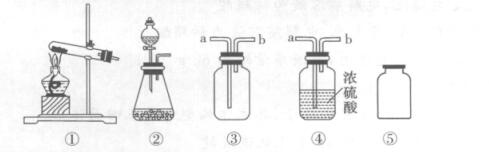
3.以下是实验室制取、收集、干燥气体的装置图,下列有关说法错误的是 ( )
 (C)
(C)
A. 实验室用氯酸钾制取氧气可使用装置①,用石灰石和稀盐酸制取二氧化碳可使用装置②
B. 实验室收集O2和CO2均可使用装置③,气体从导管a进入
C. 实验室干燥O2和CO2均可使用装置④,气体从导管b进入
D. 实验室收集的O2和CO2均可使用装置⑤临时存放
解析:实验室用氯酸钾制取氧气的反应物是氯酸钾和二氧化锰(催化剂)固体,反应条件是加热,为固固加热反应制取气体,可使用装置①;石灰石和稀盐酸制取二氧化碳,为固液常
本文档预览:3000字符,共12682字符,源文件无水印,下载后包含无答案版和有答案版,查看完整word版点下载