
中学教师资格考试(高级化学学科知识与教学能力)模拟试卷46
单项选择题
1.下列有关叙述正确的是( )。(C)
A. 电解质的导电性和金属晶体的导电性都随温度的升高而降低
B. “加碘食盐”“高钙牛奶”“含氟牙膏”“富硒营养品”等,这里的碘、钙、氟、硒指的是分子
C. “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
D. 电解水制取氢气和氧气时,通常加入氯化钠等强电解质
解析:电解质的导电性随温度的升高而升高,但金属晶体的导电性随温度的升高而降低,两者的导电性随温度的变化是不一样的;“加碘食盐”“高钙牛奶”“含氟牙膏”“富硒营养品”等,这里的碘、钙、氟、硒指的是元素;“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高;电解水制取氢气和氧气时,通常加入硫酸钠等强电解质,增强溶液的导电性,加入氯化钠,在阳极会产生Cl2,影响O2的生成。
2.用NA表示阿伏加德罗常数值。下列判断正确的是( )。(C)
A. 28 g N2含有的共用电子对数目为NA
B. 常温常压下,22.4 L Cl2含有的分子数为NA
C. 1 mol Na与足量乙醇反应时失去的电子数为NA
D. 1 L 1 mol.L-1 K2CO3溶液含有的CO32-数目为NA
解析:28 g N2的物质的量是1 mol,含有的N2的分子数为1 mol,每个N2分子含有3对共用电子,因此28 g N2含有的共用电子对数目为3NA;常温常压下,22.4.L Cl2的物质的量不是1 mol,所以常温常压下22.4.L Cl2含有的分子数不是NA;1 mol Na与足量乙醇反应时失去的电子数为NA;由于K2CO3是强碱弱酸盐,CO32-在水溶液中会发生水解,所以1 L 1 mol.L-1 K2CO3溶液含有的CO32-数小于NA。
3.下列溶液中微粒浓度关系正确的是( )。(C)
A. 含有NH4+、Cl-、H+、OH-离子的溶液中,其离子浓度一定是c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B. 常温下,pH=8的氨水与氯化铵的混合溶液中:c(Cl-)>c(NH4+)
C. 0.1 mol.L-1的Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S)
D. 常温下pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH-)=c(H+)
解析:含有NH4+、Cl-、H+、OH-离子的溶液中,可能为一水合氨和氯化铵的混合溶液,则可能存在c(NH4+)>c(Cl-)>c(OH-)>c(H+);pH=8的氨水与氯化铵的混合溶液,显碱性,则c(OH-)>c(H+),由电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-)可知,c(Cl-)<c(NH4+);由质子守恒可以知c(OH-)=c(H+)+c(HS-)+2c(H2S);pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液与酸的强弱有关,当酸是弱酸时,则c(OH-)<c(H+),当酸是强酸时,才存在c(OH-)≤c(H+)。
4.如表格所示,为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是( )。
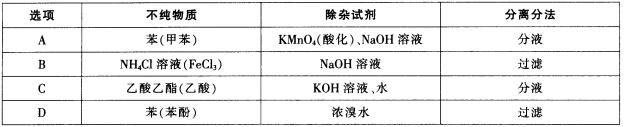 (A)
(A)
A.
B.
C.
D.
解析:苯中混有的甲苯容易被酸化的KMnO4溶液氧化为苯甲酸,然后利用酸碱中和反应,用NaOH溶液中和苯甲酸,再利用苯不能溶于水,而苯甲酸钠溶于水的性质,通过分液的方法分离得到;NH4Cl溶液中混有FeCl3,若加入NaOH溶液,二者都会发生反应,同时会引入新的杂质Na+,所以不能达到分离的目的;乙酸乙酯中混有乙酸,若用:KOH溶液,酯会发生水解反应;浓溴水与苯酚反应生成2,4,6-三溴苯酚沉淀,但溴单质和2,4,6-三溴苯酚均易溶于苯,无法用过滤的方法分离。
5.盐酸乙哌立松片(Eperisone Hydrochloride Tablets)是一种骨骼肌松弛剂,能改善由肩周炎、腰痛症等引起的肌紧张状况。其结构简式如下: