
中学教师资格考试(高级化学学科知识与教学能力)模拟试卷50
单项选择题
1.NA是阿伏加德罗常数。下列说法正确的是( )。(A)
A. 7 g CnH2n中含有的氢原子数目为NA
B. 18 g D2O中含有的质子数目为10NA
C. 标准状况下,22.4 L CHCl3中含有氯原子数目为3NA
D. 1 L 0.5 mol/L Na2CO3溶液中含有的CO32-数目为0.5NA
解析:CnH2n的相对分子质量为14n,7 g CnH2n的物质的量为 mol,则氢原子的物质的量为2n×
mol,则氢原子的物质的量为2n×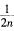 mol=1 mol,因此含有的氢原子数目为NA;18 g D2O的物质的量为
mol=1 mol,因此含有的氢原子数目为NA;18 g D2O的物质的量为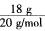
2.下列离子方程式书写错误的是( )。(C)
A. 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B. 酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
C. 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-=Mg(OH)2↓,
D. 铅酸蓄电池充电时的正极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42-
解析:等物质的量的MgCl2、Ba(OH)2和HCl溶液混合的离子方程式为Mg2++4OH-+2H+=Mg(OH)2↓+2H2O。
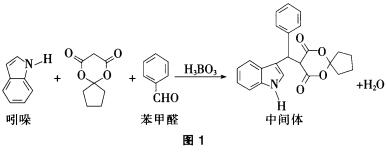
3.某抗肿瘤药物中间体的合成路线如图1。下列说法正确的是( )。
 (C)
(C)
A. 吲哚的分子式为C8H6N
B. 苯甲醛中所有原子不可能全部共平面
C. 可用新制氢氧化铜悬浊液区分苯甲醛和中间体
D. 1 mol该中间体最多可以与9 mol氢气发生加成反应
解析:由图可知吲哚的分子式为C8H7N;苯环是平面六边形,—CHO中C原子是sp2杂化,空间构型是平面形,因此苯甲醛中所有原子可能全部共平面;苯甲醛中含有醛基,能使新制的氢氧化铜悬浊液出现砖红色沉淀,中间体不含有醛基,不能使新制的氢氧化铜悬浊液出现砖红色沉淀,因此,可用新制氢氧化铜悬浊液区分苯甲醛和中间体;1 mol中间体含有2 mol苯环和1 mol碳碳双键,因此,1 mol该中间体,最多可以与7 mol氢气发生加成反应。
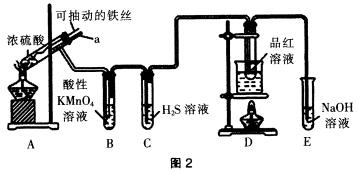
4.实验室为探究铁与浓硫酸(足量)的反应,并验证SO2的性质,设计如图2所示装置进行实验。下列说法不正确的是( )。
 (B)
(B)
A. 装置B中的酸性KMnO4溶液逐渐褪色,体现了二氧化硫的还原性
B. 实验结束后可向装置A的溶液中滴加KSCN溶液以检验生成的Fe3+
C. 装置D中的品红溶液褪色可以验证SO2的漂白性
D. 实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
解析:铁丝与浓硫酸反应生成SO2,因为酸性高锰酸钾具有强氧化性,装置B中酸性高锰酸钾溶液褪色,体现了SO2的还原性,A项说法正确;浓硫酸具有强氧化性,可能把生成的Fe2+氧化成Fe3+,因此不能检验Fe3+是否是铁丝和浓硫酸反应生成的,B项说法错误;品红溶液褪色,体现SO2的漂白性,C项说法正确;导管a的作用是使内外压强相同,防止装置B中的溶液倒吸,D项说法正确。
5.根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如图3原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol.L-1
本文档预览:3000字符,共14278字符,源文件无水印,下载后包含无答案版和有答案版,查看完整word版点下载