
教师公开招聘考试(中学化学)模拟试卷22
单项选择题
1.下列离子方程式书写正确的是( )。(A)
A. 向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2Ba2++4OH–=2BaSO4↓+AlO2–+2H2O
B. 向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O
C. 向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH4++OH–=NH3.H2O
D. 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH–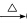 解析:B项,Fe2+能被稀硝酸氧化为Fe3+;C项,应为NH4++H2PO4–+3OH–=NH3↑+3H2O+PO43-;D项,应为CH2BrCOOH+2OH–=HOCH2COO–+H2O+Br–。
解析:B项,Fe2+能被稀硝酸氧化为Fe3+;C项,应为NH4++H2PO4–+3OH–=NH3↑+3H2O+PO43-;D项,应为CH2BrCOOH+2OH–=HOCH2COO–+H2O+Br–。
2.2008年夏季奥运会在北京举行,突出了“绿色奥运、科技奥运、人文奥运”的理念。“绿色奥运”是指( )。(C)
A. 加大反恐力度,并讲求各国运动员的营养搭配,使他们全身心投入比赛
B. 严禁使用兴奋剂,使运动员公平竞争
C. 把环境保护作为奥运设施规划和建设的首要条件
D. 奥运场馆建设均使用天然材料,不使用合成材料
解析:把环境保护作为首要条件,体现了绿色奥运。
3.下列说法不正确的是( )。(B)
A. 人类历史上使用最早的合金是青铜,目前世界上使用量最大的合金是钢
B. 从金属矿石中提炼金属一般步骤依次是:矿石的富集、精炼、冶炼
C. 硫酸的消费量常被视为一个国家工业发达水平的一种标志
D. 能源、信息、材料通常被称为新科技革命的三大支柱
解析:提炼金属要先进行矿石的富集、冶炼,最后再精炼。冶炼是从矿石中提炼出粗金属。精炼是把粗金属中没用的成分除去,变为纯度比较高的金属。
4.下列有关实验的做法不正确的是( )。(D)
A. 浓硫酸稀释时,将浓硫酸沿烧杯内壁慢慢注入蒸馏水中,并用玻璃棒搅拌
B. 用加热分解的方法区分碳酸钠和碳酸氢钠两种固体
C. 配置.1000 mol·L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流
D. 用分夜漏斗可以将乙醇和乙酸的混合物分开
解析:乙醇和乙酸互溶,不能用分液的方法将其分开。
5.将四氧化二氮置于密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色。该反应是一个可逆过程:N2O4(g) (B)
(B)
A. ②⑤⑦
B. ①③④⑥
C. 只有③④
D. 只有⑤⑦
解析:化学反应平衡的标志是正逆反应速率相同,即四氧化二氮的消耗速率与生成速率相同。四氧化二氮为无色气体,而二氧化氮为红棕色,若反应达到平衡,二氧化氮与四氧化二氮的比例不再发生变化,故烧瓶内气体颜色不再加深,反应一定达到平衡,二氧化氮的物质的量浓度亦不会发生变化。由于反应前后气体的体积发生了变化,若烧瓶内气体压强不变,反应事实上达到了平衡。根据质量守恒定律,无论反应是否达到平衡,都没有质量的损失,烧瓶的体积未变。故气体质量及密度在反应过程中均恒定不变。
有机物A县摄常用的食用油抗氧化剂,分子式为C10H12O5,可发牛如下转化:
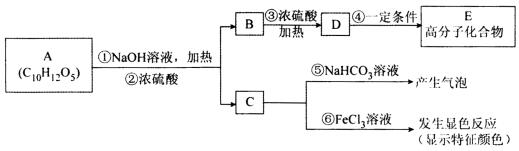
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为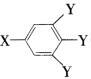
6.C中含有的官能团一X的名称为( )。(B)
A. 羟基
B. 羧基
C. 醛基
D. 烷基
解析:B的相对分子质量为60,分子中只含一个甲基,能在浓硫酸的作用下发生消去反应,则B为1一丙醇,即CH3CH2CH2OH,发生消去反应得到丙烯,即D为CH3CH=CH2,高分子化合物E为聚丙烯,C能和碳酸钠发生反应生成二氧化碳,则一定含有羧基,能和氯化铁溶液发生显色反应,一定含有酚羟基,所以C为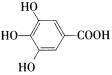 ,B和C是A发生酯的水解反应得到的产物,所以A的结构简式为
,B和C是A发生酯的水解反应得到的产物,所以A的结构简式为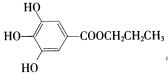
7.反应④的反应类型为( )。(C)
A. 消去反应
B. 取代反应
C. 加聚反应
D. 酯化反应
解析:B为CH3CH2CH2OH,发生消去反应生成物质D为CH3CH=CH2,D发生加聚反应生成E: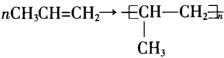
8.从分子结构上看,A作为食用油抗氧化剂的主要原因是( )。(C)
A. 含有苯环
B. 含有羰基
C. 含有酚羟基
D. 含有羧基
解析:根据苯酚在空气中易被氧化来确定,A具有抗氧化作用的主要原因是分子中有酚羟基。
9.C有多种同分异构体,其中符合要求:
①含有苯环;
②能发生银镜反应;
③不能发生水解反应的同分异构体有( )种。(C)
A. 1<
本文档预览:3500字符,共21461字符,源文件无水印,下载后包含无答案版和有答案版,查看完整word版点下载