
中学教师资格考试(初级化学学科知识与教学能力)模拟试卷52
单项选择题
1.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )。(C)
A. pH=1的溶液中:Na+、K+、MnO4–、CO32-
B. c(H+)=1×10-13mol/L的溶液中:Mg2+、Cu2+、SO42-、NO3–
C. 0.1 m01/L NH4HCO3溶液中:K+、Na+、NO3–、Cl–
D. 0.1 mol/L FeCl3溶液中:Fe2+、NH4+、SCN–、SO42-
解析:pH=1的溶液呈强酸性,含有大量的H+,与弱酸根离子CO32-不能大量共存,A项错误。c(H)=1×10-13mol/L的溶液呈强碱性,Mg2+、Cu2+和氢氧根离子生成沉淀,所以不能大量共存,B项错误。NH4HCO3和这几种离子之间不发生反应,所以能共存,C项正确。Fe3+、SCN–能生成络合物而使溶液呈红色,可以利用该反应检验铁离子,这两种离子不能大量共存,D项错误。
2.38.4 g铜与适量的浓硝酸发生氧化还原反应,铜全部反应后,在标准状况下收集到22.4 L气体,则消耗硝酸的物质的量是( )。(C)
A. 1.0 mol
B. 1.6 mol
C. 2.2 mol
D. 2.4 mol
解析:铜和硝酸反应,随着硝酸浓度的减小,硝酸的还原产物的价态降低,铜和浓硝酸反应生成NO2,而与稀硝酸反应时则生成NO2,故生成的气体有NO2和NO,则 ,即被还原的硝酸的物质的量为1 mol,
,即被还原的硝酸的物质的量为1 mol,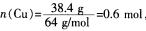
3.下列有关“化学与生活”的叙述不正确的是( )。(D)
A. 食醋可以清除水垢
B. 淀粉和蛋白质都能发生水解反应
C. 硅胶可用作食品干燥剂
D. 点燃爆竹后,硫燃烧生成SO3
解析:食醋的主要成分为醋酸(CH3OOH),水垢的主要成分为碳酸钙(CaCO3),二者反应生成二氧化碳和醋酸钙,醋酸钙溶于水,故食醋可以清除水垢,A项正确。淀粉水解为葡萄糖,蛋白质水解为氨基酸,B项正确。硅胶多孔,吸附水分能力强,且没有毒,常用作实验室和袋装食品、瓶装药品等的干燥剂,C项正确。硫燃烧生成SO2,D项错误。故本题选D。
4.下列有关实验操作、现象和解释或结论都正确的是( )。
 (D)
(D)
A.
B.
C.
D.
解析:在过量的Fe粉中加入稀HNO3,反应生成Fe2+,滴入KSN溶液,溶液不为红色,A项错误。向AgI沉淀中滴人稀KCl溶液,AgI的溶解度更小,因此不会有白色沉淀出现,B项错误。Al箔插入浓HNO中,无现象,原因是Al箔表面被浓HNO3氧化,形成致密的氧化膜,而稀HNO3会和铝箔反应生成NO气体,遇空气变为红棕色的NO2,C项错误。氨水溶液显碱性,用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,D项正确。
5.某电化学实验装置如图1所示,下列说法正确的是( )。
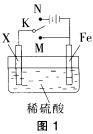 (D)
(D)
A. 若X为碳棒,开关K置于M处,则溶液中的H+移向Fe极
B. 若X为碳棒,开关K置于N处,转移0.2 mol e–时析出0.1 mol O2
C. 若X为铜棒,开关K置于M或N处,均可减缓铁的腐蚀
D. 若X为锌棒,开关K置于M或N处,锌电极上反应均为Zn-2e–═Zn2+
解析:A项中所述条件下,构成原电池,Fe极作为负极失去电子,H移向正极(即X碳棒),A项错误。B项中所述条件下,构成电解池,阳极生成氧气,电极反应为4OH–-4e–═O2↑+2H2O,转移0.2 mol e–时析出0.05 mol O2,B项错误。开关K置于M处时构成原电池,会加快铁失去电子被氧化的速度,C项错误。开关K置于M或N处,锌分别为原电池的负极和电解池的阳极,均发生反应Zn-2e–═Zn2+,D项正确。
6.普伐他汀是一种调节血脂的药物,其结构简式如图2所示(未表示出其空间构型)。
本文档预览:3000字符,共14428字符,源文件无水印,下载后包含无答案版和有答案版,查看完整word版点下载